Zrychlit vstup inovací, zajistit finanční udržitelnost systému i minimalizovat počty žádostí o úhradu přes paragraf 16 – to jsou cíle, o něž usiluje novela zákona o veřejném zdravotním pojištění, kterou nyní dokončuje ministerstvo zdravotnictví. Ze stovky inovativních léků, které v předchozích dvou letech zaregistrovala Evropská léková agentura, jich totiž v Česku nejsou dostupné téměř tři čtvrtiny, dlouho se táhnoucí řízení na SÚKL brzdí revize s potenciálem stamilionů úspor a žádosti přes paragraf 16 se staly masovým způsobem úhrady léčby. Na druhou stranu je nutno zdůraznit, že vstup léčiv má, na rozdíl třeba od přístrojů, intervencí či vakcín, jasně daná pravidla – která by se ale v závislosti na tom, jak se ministerstvu podaří paragrafové znění zákona, mohla dále zlepšit. O problematice diskutovali odborníci na konferenci Udržitelnost financování zdravotní péče, kterou uspořádala na konci dubna v Praze Academy of Health Care Management.
Léky jsou v českém zdravotnictví jedním z mála segmentů, v němž se v nějaké formě uplatňuje hodnocení zdravotnických technologií (HTA) a nákladová efektivita. Přesto má ale systém řadu much. Jak shrnuje ředitelka lékového ústavu Irena Storová, dochází dnes často k prodlevám při vstupu inovací, které jsou dány náročným administrativním procesem určeným v zákoně. Vedle toho není optimální míra zapojení risk-sharingových schémat, dopad do rozpočtu v jednotlivých případech narůstá a navíc se často ani nedodržuje.
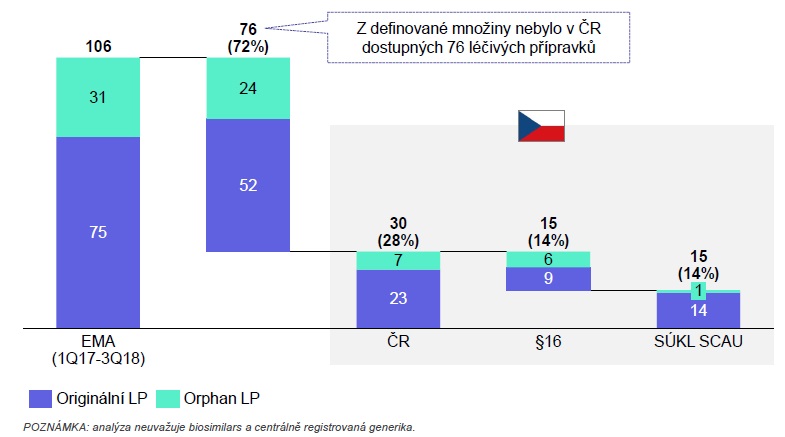
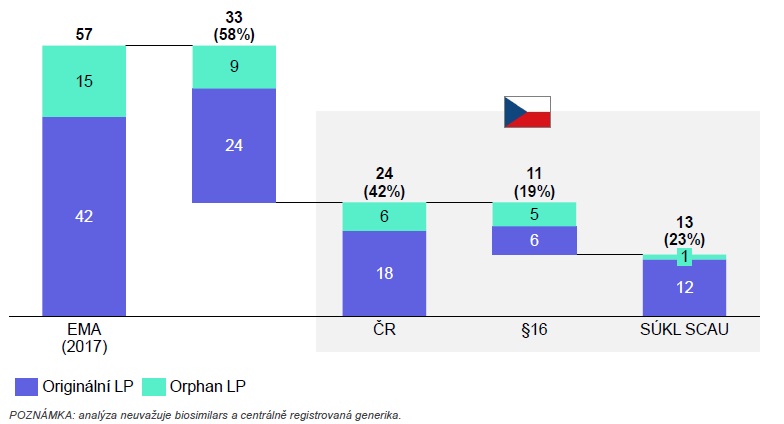
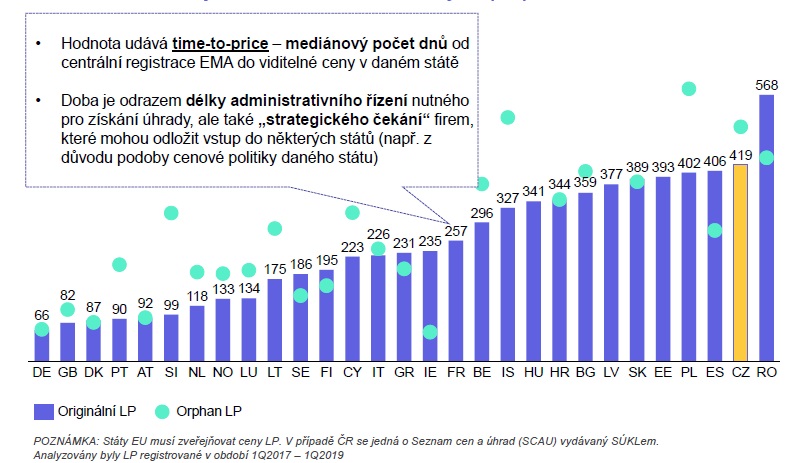
Prodlevy při schvalování a horší dostupnost nových léků podtrhuje také ředitel institutu iHETA Tomáš Doležal. Podle analýzy totiž bylo v období od prvního čtvrtletí 2017 do třetího čtvrtletí 2018 Evropskou lékovou agenturou (EMA) zaregistrováno celkem 106 léčivých přípravků, z nichž ale jen 14 procent získalo v ČR úhradu, stejný počet pak byl hrazen přes paragraf 16. Celkem 72 procent (tj. 76 nově schválených přípravků) u nás nebylo dostupných vůbec. Pokud bychom se podívali na léky schválené EMA pouze v roce 2017 (bylo jich 57), stoupne podíl těch dostupných nyní i v Česku na 42 procent (23 procent se standardní úhradou). V porovnání s ostatními zeměmi EU ve výsledku máme za Rumunskem druhý nejpomalejší přístup k nově schváleným lékům (v analýze se ale ještě neprojevilo to, že řízení na SÚKL se v posledním roce zrychlilo). Důvodem tohoto stavu jsou vedle menší atraktivity českého trhu a vlivu na ceny v jiných zemích (ČR je v referenčních koších 13 dalších států, k tomu u nás sílí tlak na zveřejňování cen) právě i dlouhé lhůty na SÚKL.
Zrychlení vstupu inovací by ovšem na druhou stranu mělo být doprovázeno i dalšími kroky. Když se totiž podíváme na novou léčbu a rozšíření indikací, předpokládá jen v letošním roce VZP 59 vstupů s dopadem během nadcházejících 12 měsíců ve výši více než 2,3 miliardy korun. Aby na tyto nárůsty byly prostředky, je třeba hledat rezervy jinde. V minulosti byly velkým zdrojem úspor revize, a i když se už jejich hlavní potenciál vyčerpal, stále ještě díky nim lze ušetřit nemalé prostředky – ovšem i zde by bylo na místě zrychlení řízení na SÚKL. „Je tam množství řízení, která stojí dva, tři, čtyři, některá i pět let. Přimlouvali bychom se tedy za vyváženost postupu u vstupu inovací, racionalizace výše úhrad a celkových dopadů,“ apeluje ředitelka odboru léčiv a zdravotnických prostředků VZP Alena Miková. Například zkrácená revize antiTNF léku a hloubkové revize rituximabu, imatinibu a nilotinibu by měly přinést potenciální úsporu ve výši 950 milionů korun. Vedle toho pak pojišťovny uzavírají prohlášení o ceně i různé typy smluv, které do systému přinášejí další úspory.
Korigovat výklady nároku pojištěnce v soudní síni není šťastné
Vedle problémů v praxi má ovšem současný stav také právní mouchy. „Přetrvává nerovný přístup k péči mezi zdravotními pojišťovnami i uvnitř jedné zdravotní pojišťovny a mezi diagnózami. Máme tu různé výklady nároku pojištěnce, které korigujeme v soudní síni, což vůbec není šťastné. Je také otázka, jaká je vůbec do budoucna role revizního lékaře versus odborné závěry ošetřujících lékařů. Slýchám totiž často výtku ze strany poskytovatelů, že jejich odborné závěry o tom, co je pro pacienta nejpřínosnější, jsou revizními lékaři revidovány,“ poukazuje přednostka Ústavu veřejného zdravotnictví a medicínského práva 1. LF Jolana Těšinová.
Právě na tuto problematiku by se přitom měla zaměřit úprava zákona 48 o veřejném zdravotním pojištění, tzv. malá procesní novela, která je nyní v připomínkovém řízení. Ta se totiž snaží zakotvit rozhodování zdravotních pojišťoven, tedy sjednotit procesní pravidla a nahradit současné pseudosprávní řízení probíhající na zdravotních pojišťovnách, které však nemá zákonné vymezení. „Není jasné, kdo je účastníkem řízení – jestli je to poskytovatel nebo i pacient, případně jakou roli v žádostech poskytovatelů sehrávají odborná vyjádření, jestli vůbec nějakou,“ dodává Těšinová. V důvodové zprávě ke zmíněné novele je přitom zmínka, že je třeba zvážit, zda není role revizního lékaře překonaná. Úloha revizního lékaře má být podle ní v podobě přezkoumávání důvodnosti a podloženosti podkladů odborníků. „Nabízí se tedy, jestli to vůbec musí být revizní lékař, když by se to mohlo redukovat na formální rovinu,“ míní Těšinová.
Další velký otazník pak je, na co vlastně má pacient v rámci žádostí na paragraf 16 nárok. Jedna z prvních žalob v tomto smyslu přišla v polovině roku 2017 a týkala se úhrady terapie u metastatického karcinomu prsu (o případu by nyní měl rozhodovat Nejvyšší správní soud v rámci kasační stížnosti). Nyní se podle Jolany Těšinové vede kolem dvacítky podobných soudních sporů.
Mohlo by vás zajímat
„Začaly se vést diskuze, které do té doby nebyly: co je vlastně nárokem pojištěnce, který patří pod paragraf 16. Ukázalo se, že to nejsou jen léky, které nemají úhradu, ale i ty, které jsou registrované, úhradu mají, ale je tam indikační omezení, do kterého se pacient nevejde. Začala se také aktivně rozvíjet debata, co je jediná možnost léčby, kterou v sobě paragraf 16 skrývá – jestli je to jen léčba, která nemá alternativu, nebo jde i o to, co dnes od léků očekáváme, tedy že i významně ovlivní kvalitu života, mají vyšší terapeutický účinek, případně zda tam patří i vyšší komfort léčby. Kritériem je také výjimečnost situace, a i to je předmětem diskuzí a soudního posuzování. Je výjimečnou okolností těhotenství, alergický stav, věk, četnost onemocnění nebo zařazení pacienta do studie, která končí a není nikdo, kdo by následně léčbu hradil?“ načrtává Těšinová.
Podle několika rozhodnutí městských soudů, která jsou dosud k dispozici, namůže výjimečně hrazená péče nabýt charakteru systémového opatření jdoucího nad obecné limity péče. Limitující kritérium omezeného objemu finančních prostředků ale nesmí být uplatňováno způsobem znamenajícím v důsledku diskriminující či libovolné podmínky pro přístup k hrazené péči. Pod paragraf zároveň nelze podřadit pouze situace, kdy pojištěnec nemůže využít žádnou alternativu hrazené léčby, ať už z důvodu, že pro danou indikaci žádný hrazený lék neexistuje, nebo kvůli alergii či jiné nesnášenlivé reakci – to by totiž jeho využití ve většině případů znemožnilo. Na druhé straně to ale neznamená, že již samotná existence léku vykazujícího vyšší terapeutický účinek by v dané indikaci měla být rozhodující pro naplnění kritéria jediné možnosti, protože by tak bylo znemožněno zohlednění nákladové efektivity.
„Jednoznačně ze závěrů vyplývá, že nelze postupovat restriktivně, musí být postupováno individuálně bez jakékoliv paušalizace. Nicméně jde zatím pouze o dílčí rozhodnutí městského soudu v konkrétních případech, kterých je velmi málo, a jakákoliv velká zobecnění jsou předčasná – musíme si počkat na rozhodnutí soudů vyšších,“ shrnuje Těšinová s tím, že další vodítko lze čekat v návaznosti na ústavní stížnost skupiny senátorů ohledně způsobu úhrady a nerovnosti přístupu k péči v rámci některých ustanovení zákona o veřejném zdravotním pojištění.
Režim VILP urychluje vstup inovací o roky, ukázala analýza
Napravit situaci, která vedla k růstu počtu žádostí o úhradu přes paragraf 16, se nyní snaží další, „velká“ novela zákona o veřejném zdravotním pojištění, která by měla brzy zamířit do připomínkového řízení. Hlavní důvody, proč dnes musí pojišťovny řešit tolik žádostí přes paragraf 16, jsou přitom tři: pomalý průběh správních řízení na SÚKL, nemožnost standardního vstupu pro nákladné léky zejména na vzácná onemocnění, které nesplňují nákladovou efektivitu, a off-label indikace. Cílem novely tak je zrychlit a usnadnit vstup inovativních léků do úhrad, což souvisí i s odbřemeněním SÚKL od zbytečné administrativy, a zajistit udržitelné financování.
Hlavními novinkami novely bude zavedení nové cesty schvalování pro léky, které jsou určeny jen pro velmi úzkou skupinu pacientů (tzv. ultraorphany) a rozšíření režimu pro vstup vysoce inovativních léků (VILP) z 2+1 roku na 3+2 roky (podrobně jsme psali zde). „To považuji za velice správné a jsme tím hodně progresivní. Neměli bychom systém VILP zbořit, protože umožňuje vstup inovativních léků o roky dříve, než kdyby tu systém nebyl,“ uvádí Tomáš Doležal.
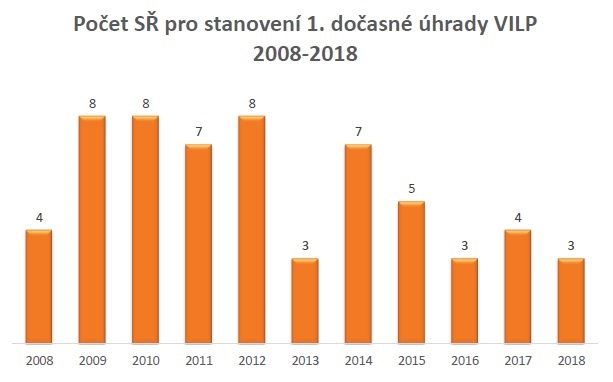
To také dokládá analýza, která byla na podzim loňského roku publikována v časopise Value in Health Regional Issues a v jejímž rámci bylo za období od roku 2008 do 2018 zkoumáno 50 VILPů (68 procent léků bylo onkologických, 44 procent orphanů). Důvodem přiznání dočasné úhrady byla nejčastěji neexistence alternativy nebo významně vyšší účinnost. Při vstupu do režimu VILP přitom měly přípravky velmi vysoký ICER (tj. poměr inkrementálních nákladů a přínosů, Incremental Cost-Effectiveness Ratio) – průměrně 2,47 milionu korun, zatímco hranice ochoty platit se u nás pohybuje kolem 1,2 milionu korun. Když ale vstupovaly do trvalé úhrady, měly ICER výrazně nižší – pohyboval se kolem 860 tisíc. Trvalou úhradu přitom získalo 83 procent léků v režimu VILP.
Skutečností, na kterou by měla reagovat i chystaná novela, ovšem je, že do režimu VILP se v posledních letech hlásí méně léků. Pro některé výrobce totiž ztratilo smysl touto cestou léky na trh uvádět. Nový systém by proto dle farmafirem měl být zpřesněn a nastaven tak, aby dál neutahoval šrouby, na druhou stranu se však ministerstvo chystá náklady na léky v tomto režimu limitovat.
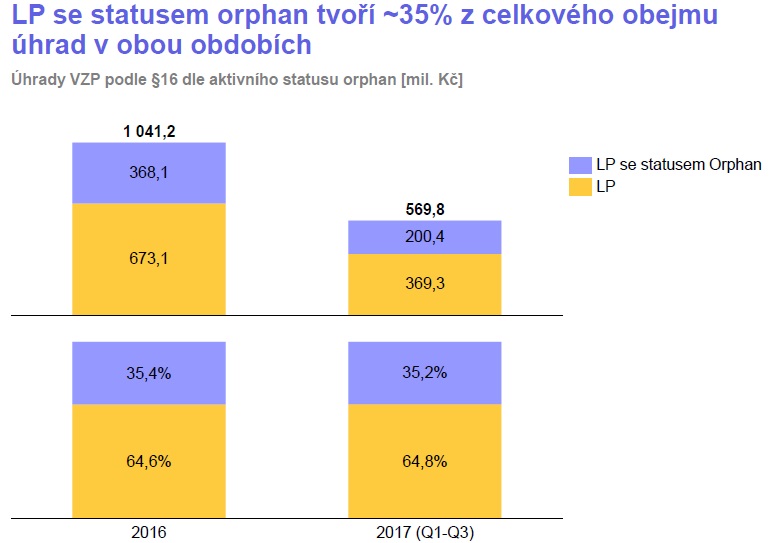
Zcela novým způsobem pak bude řešen vstup léků na vzácná onemocnění. Zhruba třetina léků hrazených dnes přes paragraf 16 jsou totiž podle Tomáše Doležala právě přípravky se statusem orphanu, což znamená, že vůbec nejdou do českého systému úhrad, protože nemají šanci splnit hranici ochoty platit. Podíl léků se statusem orphan ve standardních úhradách přitom klesá – v roce 2009, kdy bylo na našem trhu 35 orphanů, šlo 82 procent těchto léků cestou standardního schválení úhrady (v podílu nákladů šlo o 99 procent) a 18 procent cestou individuální, zatímco v roce 2017, kdy u nás bylo 50 orphanů, byl již poměr zcela jiný – standardní úhradu mělo 45 procent orphanů (v balíku nákladů 72 procent) a 55 procent šlo individuální cestou.
Zlepšit stav by měla právě chystaná nová cesta pro vstup tzv. ultraorphanů. „Já ji velmi vítám, protože je odpovědí na nedostatek systému zvláště u ultranákladných léků na vzácná onemocnění. Neznáme ale ještě paragrafované znění, a jak se říká, ďábel je v detailu. Tady je těch čertíků poměrně hodně,“ konstatuje Tomáš Doležal.
Jedním takovým otazníkem je limit stanovující to, pro kolik pacientů má být ultraorphan určen – nyní je nastaven na sto nemocných v republice. „Jsou tu vzácná onemocnění, kterým sto pacientů nebude stačit,“ míní Doležal. Důležité zároveň je, jaká kritéria bude komise, která má mít rozhodování o úhradě na starosti, zohledňovat – od nákladové efektivity a platebních schémat přes účinnost a bezpečnost po celospolečenské dopady a vliv na okolí pacienta. Na to, jak se ministerstvo s těmito otázkami popasovalo, si ale ještě budeme muset pár týdnů počkat.
Michaela Koubová