Před více než deseti lety přišel Ústav hematologie a krevní transfuze (ÚHKT) s vizí: vyrobit inovativní terapii pro hematoonkologické pacienty, kteří by se k ní jinak nedostali. Dnes už projekt nese první ovoce. A ukazuje, že když se spojí výzkum s praxí u lůžka, je možné vyvinout vlastí genové a buněčné terapie, které jsou levnější než komerčně vyráběné produkty a pacientům je lze podat rychleji. Problematice se věnovalo sympozium Zdravotnického deníku na téma Genové a buněčné terapie v Česku.
Když v roce 2012 na konferenci Americké společnosti pro hematologii lékaři představili případ první pacientky vyléčené z chronické lymfatické leukémie pomocí CAR-T terapie, propukl celosvětový zájem o buněčnou a genovou léčbu. O tři roky se k horečce rozhodl přidat také český Ústav hematologie a krevní transfuze.
„Za 10, 11 let jsme se dostali z toho, že jsme zdědili jedny čisté prostory (dobře izolované a aktivně čištěné prostory chráněné před kontaminací a splňující jasně definované podmínky tak, aby tu mohl probíhat výzkum, vývoj a výroba, pozn. red.), které ale vlastně ani pořádně čistými prostorami nebyly a musely se poměrně složitě předělávat, k tomu, že máme vlastní produkty, které podáváme pacientům. To byl přesně náš cíl,“ říká ředitel ÚHKT Pavel Cetkovský.
Během CAR-T terapie se pacientovi odeberou T-lymfocyty, které se pak pošlou do laboratoře ke genetické modifikaci. Během ní se do nich vloží chimérický antigenní receptor neboli CAR. Namnožené buňky se pak formou infuze vrátí pacientovi.
Pětičlenná farmafirma
Na počátku vyhlásilo vedení ÚHKT projekt Vize 2030, jehož cílem byl start vlastního imunoterapeutického programu. A to nejen v rámci akademického výzkumu a grantů, ale s výrobou pro pacienty.
„Základní podmínka byla, že pacienti ÚHKT musí z celého výzkumu přímo benefitovat. Potřebovali jsme silný tým s někým, kdo rozumí výzkumu a CARům, což byl pan doktor Pavel Otáhal. A také se skvělým klinickým lékařem, panem doktorem Janem Vydrou, který je nyní přednostou. Já se starám o to, aby věci fungovaly,“ popisuje vedoucí oddělení imunoterapie Petr Lesný.
Mohlo by vás zajímat

Prvním úkolem byla příprava výrobního projektu, který prokáže schopnost pracovat v systému správné výrobní praxe. V podstatě šlo o založení miniaturní pětičlenné farmaceutické firmy uvnitř ÚHKT. Tým si přitom potřeboval vyzkoušet, zda dokáže to, co velká farmafirma. Tedy výrobu CAR-T terapií cílených na antigen CD19.
Z výzkumu k pacientům, od pacientů do výzkumu
Od roku 2015 do 2019 tak běžela rekonstrukce čistých prostor a první studie s NK buňkami (natural killer cells, tedy přirození zabíječi, jsou bílé krvinky vrozené imunity, které okamžitě identifikují a ničí rakovinné nebo virem infikované buňky. Lze je přitom aktivovat a přenést zpět do dárce).
„Pod hlavičkou imunoterapeutické skupiny se nám povedlo implementovat kolečko translačního výzkumu, které se pořád musí točit. Výzkum něco vyzkoumá a přejde to do praktického použití. Se zkušeností na pacientech se to vrací zpátky do výzkumu, kde se vyvíjí nová generace. Dnes jsme u NK buněk u třetí generace produktu a ve výzkumu je pátá generace. Financování probíhá z grantů nebo darů,“ přibližuje Lesný.
Podle něj se povedlo nastavit fungování tak, že vědci rozumí i klinickým problémům. Lékaři v klinické praxi zase zvládnou formulovat zadání pro vědce – a kontrolovat jejich výstupy.
Vylepšené a v nových indikacích
V roce 2019 dostal ústav první povolení k výrobě přípravků genové terapie. O dva roky později pak dostal zelenou k prvnímu klinickému hodnocení s původním přípravkem vyvinutým v Česku.
„To už bylo v době, kdy v ČR byly komerční CAR-T přípravky. Naše klinické hodnocení tak probíhá pořád, protože dostáváme pacienty v horším klinickém stavu, kteří nejsou indikováni pro komerční CARy,“ doplňuje Petr Lesný.
Jako první začal ústav produkovat CAR-T proti CD19. Těch je ale nyní komerčně k dispozici řada, takže se jim už tolik nevěnuje. „Nechceme je ale zcela opustit. Rádi bychom je vylepšili. A proč je nepoužít v dalších indikacích – otevírá se nejen hematologie, ale revmatologie, dermatologie a další a další. A pak se soustředíme na další cíle, které zatím nejsou komerčně dostupné, hlavně u AML (akutní myeloidní leukemie, pozn. red.),“ přibližuje ředitel Cetkovský.
Povede se přípravky licencovat?
V roce 2024 se povedlo v patřičné kvalitě vyrobit CAR-T proti antigenu CD123 u pacientů s akutní myeloidní leukémií před transplantací. Loni pak odstartovalo klinické hodnocení u lidí. Čeští pacienti se tak dostanou k terapii, k níž by jinak neměli přístup.
„Umožňuje nám to povídat si s farmaceutickými firmami na vyšší úrovni, než kdybychom dělali čistý výzkum. V okamžiku, kdy pošleme farmaceutické firmě odkaz na clinical trial´s goal, kde máme registrovaná naše klinická hodnocení, začínáme uvažovat o tom, že bychom mohli být v něčem partneři, mohlo by u nás probíhat first-in-human klinické hodnocení něčeho zajímavého, ale mohli bychom také začít jednat o licencování některého z genetických konstruktů,“ načrtává Lesný.
Výroba u lůžka pacienta má přitom podle něj nepopiratelné výhody. Odpadá totiž složitý management a logistika, kterou si vyžadují komerční přípravky vyráběné v zahraničí. Podle Lesného by tak pro farmafirmy bylo jednodušší prodávat výrobu vektoru pracovištím, která pak výrobu u lůžka zvládnou.
Ve hře je i ambulantní podání
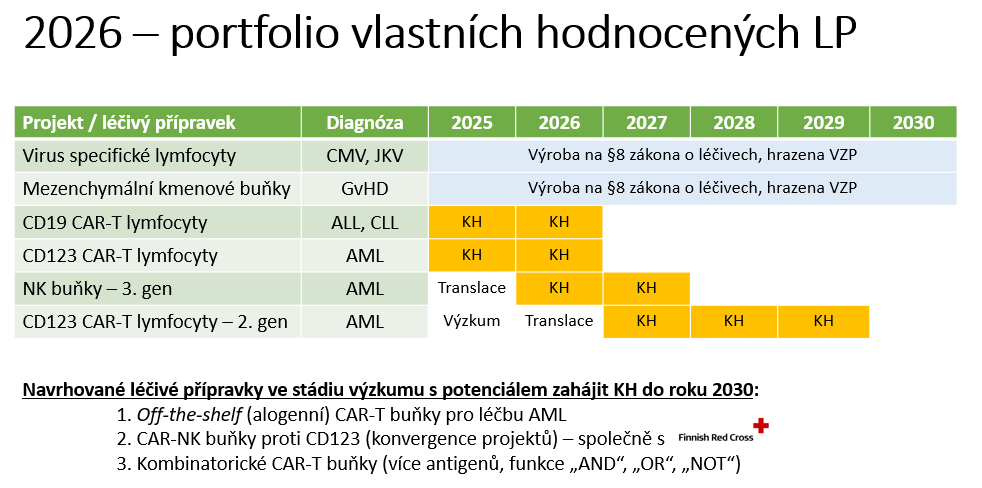
Už letos má přitom ústav v úhradě od pojišťoven virus specifické lymfocyty a mezenchymální kmenové buňky. Vedle končící studie s CAR-T proti CD19 běží studie proti CD123 a u NK buněk v třetí generaci vývoje s vylepšenou efektivitou.
„A začíná velmi ambiciózní projekt 10denních 123 CARů. To znamená vein-to-vein time 10 dní (tedy od odebrání buněk pacienta do infuze upravených buněk, pozn. red.). To je u AML poměrně důležité a jde o vlastnost, kterou klinici poptávají, aby mohli léčit efektivně,“ doplňuje Lesný.
Zařazování pacientů do studií ovšem podle Pavla Cetkovského naráží na omezené lůžkové kapacity. Proto by podle něj mělo být ve hře i ambulantní podávání CAR-T terapií. „Podali jsme jich hodně přes stovku, umíme s tím zacházet. A i na kongresech už vidíme, že mají soubory pacientů nad 75 let, kterým to bylo podáno ambulantně. 30 až 40 % z nich hospitalizaci kromě vlastního podání vůbec nepotřebuje. Vracejí se jen v případě komplikací,“ konstatuje Cetkovský.
Kývnou pojišťovny na CAR-T výrobu u lůžka?
Každopádně CAR-T terapie se budou podle Lesného stávat součástí evidence-based medicíny čím dál častěji. Abychom léčbu zvládli ufinancovat, mohli bychom se podle něj inspirovat ve Španělsku, kde jsou tyto terapie hrazeny jako součást nemocniční výjimky.
„ÚHKT může nabídnout vývoj nových CAR-T a NK buněk. Aktivně spolupracujeme jak s pracovištěm v Ostravě, tak v Brně, kde společně vyvíjíme nové přípravky. Pojišťovnám bychom tak mohli s našimi unikátními zkušenostmi nabídnout, že bychom dokázali zorganizovat pilotní program výroby CAR-T u lůžka pacienta,“ dodává Lesný s tím, že pilot by byl za cenu nákladů.


















