Akutní myeloidní leukémie je jedním ze čtyř základních typů leukémií, která bez terapie připraví pacienta o život do pár měsíců. Její léčba je přitom velmi náročná, protože jde o variabilní onemocnění, na něž není lehké specificky cílit. Jako velmi slibná u lidí, kde už jiná léčba nezabírá, se nyní jeví buněčná imunoterapie. Právě na ni se zaměřují také odborníci z Ústavu hematologie a krevní transfúze (ÚHKT). Jedním ze směrů, který tu nyní začínají zkoumat, je vývoj buněčné terapie používající takzvaných přirozených ničitelů, což jsou buňky likvidující buňky nádorové. Historicky vůbec poprvé se přitom ÚHKT povedlo získat významného sponzora ze soukromého sektoru, průmyslově-technologický Holding Czechoslovak Group. O výzkumu a o tom, jak bude projekt, na který CSG přispělo pět milionů korun, vypadat, si ZD povídal s vedoucím oddělení výzkumu moderní imunoterapie Janem Fričem a tajemnicí ředitele ÚHKT Andreou Daňkovou.
Věda a výzkum jsou jedním z pilířů činnosti ÚHKT. Na co všechno se ústav v tomto směru zaměřuje? Kde je těžiště jeho výzkumné činnosti?
AD: Spektrum je velmi široké, ale gró posledních let je moderní imunoterapie a procesy s ní spojené.
JF: Hlavní zaměření výzkumu můžeme rozdělit na několik pilířů. Jedním je dlouhodobě výzkum úzce navázaný na diagnostiku a monitorování průběhu onemocnění. Věnujeme se mutacím a tomu, jak různé mutace detekovat a případně na ně cílit další léčbu. Výzkumná oddělení se zaměřují také na různé inhibitory, které cílí na leukemické buňky a další v praxi používaná a nebo vyvíjená léčiva. Pomáháme tak vytvářet znalosti k vývoji nových přípravků, případně optimalizovat využití těch stávajících. Oblastí, která se nyní hodně rozvíjí, je imunoterapie, zvláště ta buněčná. V ÚHKT vzniklo několik nových oddělení, která se specificky zabývají vývojem léčivých přípravků založených na buňkách. Můžeme je rozdělit na několik typů. Buď se snažíme vyvíjet specifické přípravky založené na transgenních T-buňkách, což jsou například CAR-T terapie. Další možností jsou nespecifické přípravky, které využívají přirozené protinádorové vlastnosti některých buněk, například NK buněk (tj. natural killers čili přirození ničitelé, pozn. red.). Dále pak probíhá výzkum vzácných hematologických onemocnění, souvisejících se vzácnými mutacemi či poruchami krvetvorby nebo hemostázy. V některých těchto oblastech je ÚHKT přinejmenším v Čechách unikátním pracovištěm – výzkum ani diagnostika jinde neprobíhá a máme obrovskou spádovou oblast.
Můžete přiblížit, jak buněčné imunoterapie vypadají – jak ty specifické, tak nespecifické? V čem se liší od „běžné“ léčby, například chemoterapie?

JF: U buněčné terapie se vždy odebírají nějaké buňky, které se po namnožení nebo dalších úpravách podávají pacientovi. Výjimkou jsou specifické protokoly, kdy se snažíme imunitu povzbudit protilátkami nebo jiným přípravkem. V ÚHKT je jedním z hlavních hematoonkologických onemocnění, která tu léčíme, akutní myeloidní leukémie (AML). Velká část výzkumu tak směřuje k potenciální léčbě právě tohoto onemocnění. AML je ale specifická tím, že je hodně variabilní a i po vyléčení se často vrací. Jde o plastické onemocnění, kde nejsme přesně schopni definovat znaky leukemických buněk, jako je tomu třeba u B lymfomů. CAR-T terapie cílí na jednu molekulu, proto jsou tak úspěšné u leukémií s jasně definovaným povrchovým znakem, na který buněčná terapie cílí. Jenže u AML je množství znaků proměnlivé a stále se nepřišlo na to, na který znak má smysl cílit. Kromě velké škály projektů, které se snaží definovat tyto znaky důležité pro cílenou léčbu AML, se také zaměřujeme na projekty zkoumající nespecifickou imunitu. Pokud se podíváme na NK buňky, to jsou buňky vrozené imunity, které mají v těle hlavní úkol vyhledávat nádorově pozměněné buňky a ničit je. My si myslíme, že když se nám NK buňky podaří expandovat a vrátit v dobrém stavu pacientovi, budou zase vykonávat tuto svou přirozenou úlohu a automaticky vyhledávat a zabíjet nádorově poškozené buňky. Do NK buněk tedy nepotřebujeme vkládat další geny, jen je namnožit a připravit do stavu, kdy budou co nejlépe funkční a přežijí v krevním oběhu po adoptivním transferu pacientovi.
Když to tedy laicky shrnu – pokud zachytíte leukemickou buňku, musíte u specifické buněčné terapie zjistit, co by na ni mohlo platit?
Mohlo by vás zajímat
JF: Vlastně ano. U všech leukemických typů se ve výsledku ví, který typ buňky a v jakém stadiu svého vývoje zmutoval, začal se nekontrolovaně množit a způsobil leukémii. U AML je jich větší množství, navíc každý pacient může mít mutace různé.
O kolika pacientech v ÚHKT hovoříme?
JF: U AML je to ročně necelá stovka pacientů.
Nízký počet pacientů a vysoká variabilita nemoci tedy léčbu ještě komplikuje…
JF: Ano.
Na jaké AML pacienty bude zaměřena buněčná imunoterapie?
JF: AML velice často relabuje. Návraty nemoci jsou často těžko zvládnutelné. Léčba pokračuje po několika liniích, pokaždé trochu pozměněná. Reflektuje, jaké jsou tam mutace a jaký je to typ nemoci. Jeden z projektů kolegů má za cíl připravit klinické hodnocení, ve kterém bychom podávali NK buňky preventivně pacientům v remisi tak, aby se nemoc nevrátila. NK buňky by měly zajistit prevenci proti relapsu. Buňky by se tedy podaly pacientovi, který je zrovna vesměs zdravý, a měly by zabránit návratu nemoci.
Jak vlastně výzkumnou činnost ústav financuje?
AD: Převážně z vlastních zdrojů a případně ze získaných grantů, a také z financí na podporu výzkumu od ministerstva zdravotnictví. A teď prvně navazujeme spolupráci s externí firmou. Je to historicky poprvé, kdy nám externí firma spolufinancuje projekt.
JF: To, že máme financování heterogenní, z různých typů zdrojů, nám umožňuje dosáhnout větší stability financování, která je pro výzkum velmi důležitá. Potřebujeme výhled ve víceletém horizontu. Takto nám další zdroje pomáhají překlenout období, kdy je například slabší financování z grantů a podobně.
Jaké nyní běží v ÚHKT klinické studie?
AD: Aktuálně máme 14 komerčních klinických studií a další čtyři jsou ve fázi jednání. Akademických studií je celkem šest. Dále v současnosti probíhá klinická studie s naším vlastním léčivým přípravkem, který se vyrábí v ÚHKT. Jedná se o tzv. CD19 CAR-T buňky a tato studie je plánována pro šest až deset pacientů. Jedná se o první podání produktu pacientovi, takže se provádí na malém počtu, abychom eliminovali všechna možná potencionální rizika. Tento přípravek byl již podán dvěma pacientům a zjistili jsme, že buňky u pacientů přežívají, fungují, jak mají, a nemají zásadní nežádoucí účinky. Jsme tedy snad na dobré cestě. Jedná se o první studii v České Republice, kde jsou použité buňky vyvinuté ve vlastních laboratořích a přímo podané na naší klinice, jedná se o velký úspěch dlouhodobého výzkumu vedeného doktorem Otáhalem a panem primářem Vydrou, samozřejmě za plné podpory a záštity pana ředitele profesora Cetkovského.
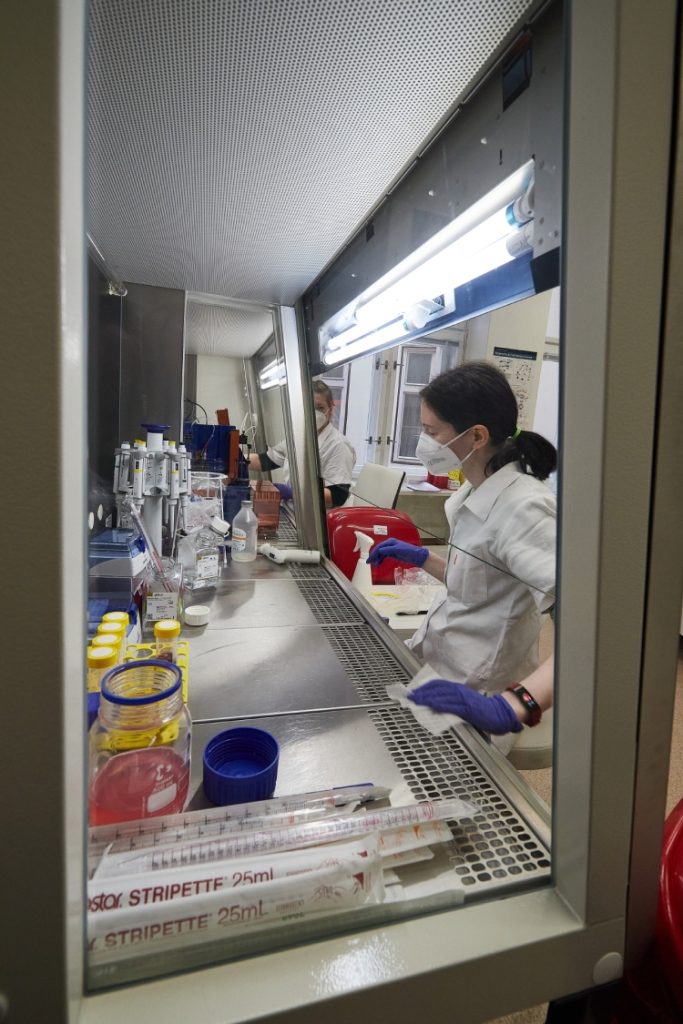
Co je k výrobě buněčných terapií zapotřebí?
AD: Jednou ze zásadních podmínek jsou čisté prostory, které máme v klinickém pavilonu. Jedná se o velmi speciální výrobní laboratoř, kde lze tyto buňky připravovat podobně, jako se vyrábějí komerční přípravky, ale s výrazně menší kapacitou. V těchto prostorách se pracuje s geneticky upraveným biologickým materiálem, a proto se musí dodržovat velmi přísná pravidla. Byli jsme jedním z prvních, kdo je u nás měl. Nyní navíc stavíme nový pavilon progresivní medicíny, kde budeme mít další čisté prostory, které nám umožní zvýšit kapacitu výroby.
Jak dlouho celý proces výroby buněčné terapie trvá?
AD: Nejprve se musí zjistit, zda pacient splňuje všechny podmínky pro léčbu – například že má dostatečné množství buněk v krvi. Pak se mu odebere krev, z níž se buňky připraví. To trvá asi tři týdny. Následně se vyrobené CAR-T buňky zamrazí a provede se několik speciálních testů, aby se zjistilo, že vše bylo vyrobené správně – to trvá asi měsíc. Celkem to trvá jeden až dva měsíce.
Tím, že terapii vyrábíte přímo na místě, navíc asi vzniká časová úspora, než je tomu v případě komerčních terapií, které se posílají do zahraničí.
AD: Výroba komerčních buněk je nejen velmi drahá, ale také organizačně velmi komplikovaná – v začátcích výroba probíhala v USA, což znamenalo, že se letecky posílal kontejner s tekutým dusíkem, ve kterém byly zamrazené buňky. Nyní se už neposílají přes oceán, ale pouze po Evropě, což je ale stále procesně velmi složité a pomalé jak z důvodu dopravy, tak byrokratické zátěže. Navíc tu jsou jednání s pojišťovnou, která musí schválit každého pacienta. Pokud bychom tedy byli schopni studie zdárně dokončit, bylo by to pro ústav velmi průlomové a umožnilo by to poskytnou tuto speciální léčbu více pacientům.
JF: Problém je, že část pacientů se pak už k přípravku nedostane. I pár dní, které ušetříme výrobou u nás, může hrát roli. Navíc na vlastním produktu můžeme snáze pokračovat v dalším výzkumu.
Jak také poukázal na jednom z kulatých stolů ZD ředitel ÚHKT Petr Cetkovský, je zároveň tady vyrobená léčba levnější než komerční terapie.
AD: Tím, že je to zatím v tak malém měřítku a navázané na výzkum, to nemáme přesně spočítané. Nicméně jiná akademická pracoviště vyrábějí podobné produkty zhruba za čtvrtinu ceny v porovnání s komerčním přípravkem. V rámci našich možností to také vyrábíme levněji, nicméně v tom není zahrnuta cena za výzkum a vývoj. Zatím je to však v první fázi, kdy se testuje bezpečnost. Jsme tedy v počátcích, ale přesto je to v našem prostředí unikátní.
Můžete popsat, jak přesně proces výroby buněčné terapie probíhá?
JF: U NK buněk plánujeme vzít buňky od příbuzného dárce, aby byl štěp haploidentický. Pak se buňky namnoží v kultuře, což trvá zhruba dva týdny. Poté se zamrazí, nebo se v případě potřeby rovnou podávají. Výzva protokolu spočívá hlavně ve standardizaci a spolehlivém namnožení dostatečného množství buněk, někdy totiž nechtějí tak dobře růst.
Když je pak pacientovi podáte, má to nějaká rizika?
JF: Zatím tolik zkušeností u nás nemáme, ale obecně každé podání těchto buněk představuje řadu rizik, a proto musí být pacient pečlivě monitorován. Může se také stát, že buňky relativně rychle zmizí nebo se neuchytí, to se ale všechno zjistí z klinických studií – u NK buněk v Česku zatím nebylo tolik podání, aby z toho šlo dělat závěry. Více zkušeností máme u T-lymfocytů a komerčních přípravků, na kterých se učíme.
Jaké jsou hlavní rozdíly mezi léčbou NK buňkami a za pomoci CAR-T terapií?
JF: U CAR-T terapie mají buňky vnesený receptor, tedy genetickou informaci pro určitou molekulu, která se vystaví na povrchu buňky a navede ji specificky k leukemické buňce, kterou cytotoxicky zničí. Specificky tedy rakovinnou buňku najde a zabije, protože jde o T-buňky, které mají cytotoxickou aktivitu. Oproti tomu u NK buněk není potřeba vkládat žádný receptor. Využíváme toho, že NK buňky si leukemickou buňku umí najít samy na základě sady informací, které mají leukemické buňky na svém povrchu. Vyhledávání nádorových buněk je přirozenou vlastností NK buněk.
Společnost CSG, která je prvním soukromým partnerem spolufinancujícím výzkum v ÚHKT, se rozhodla podpořit pěti miliony vývoj buněčné terapie používající přirozených ničitelů. Ústav se tak bude snažit vyvinou optimální metodu produkce buněk pro imunoterapii a aplikaci pacientům s leukémií. Proč padla volba právě na tuto oblast?
AD: CSG se zapojila, protože právě v tomto novém směru vidí budoucnost léčby leukémie. Společnost nabídla ÚHKT spolupráci, mimo jiné i proto, že vidí jeho vědecký potenciál a ví, že se jedná o jednu z nejvýznamnějších institucí v oblasti léčby leukémie v Česku, která na jediném místě řeší léčbu pacientů, výzkum i výrobu léčebných přípravků. Buněčná terapie může pomoci pacientům s nádory, na které dosavadní metody, tedy chemoterapie a transplantace kostní dřeně, nestačí – tuto pomoc tedy nevnímáme jen jako dar, ale jako závazek posunout projekt léčby leukémie pomocí “natural killers“ maximálně dopředu.
Jak by měl vypadat projekt podpořený CSG?
JF: Souvisí to s tím, o čem jsme hovořili, že je výzvou NK buňky namnožit. Projekt se bude zaměřovat na testování různých přístupů a strategií, jak expanzi zlepšit. Další důležitý aspekt projektu je, že nám finance umožní vyvíjet sofistikovanější modely, jak buňky testovat a ověřovat jejich cytotoxickou kapacitu. Modelů totiž není dostatečné množství. Naprostá většina výzkumu bude probíhat na krvi, kterou dostaneme ze zdravých dárců. Izolujeme z ní NK buňky a dál s nimi budeme pracovat, testovat různé protokoly expanze a pak i cytotoxické modely in vitro. Závěrem bychom po několika letech měli na základě nejlepšího protokolu vyvinout nejvíce cytotoxické buňky s vysokou fitness, které vydrží v krevním oběhu po adoptivním transferu pacientovi. Na základě toho bychom chtěli navrhnout vlastní klinické hodnocení. Mezi výzkumem v laboratoři a klinickým hodnocením je důležité mít možnost přenést laboratorní produkt do čistých prostor a standardizovat. To obnáší velké množství energie a lidských zdrojů. Část peněz z projektu tak půjde na to, abychom produkt byli schopni přenést do výroby, s čímž má ale ÚHKT již velké zkušenosti.

Jak dlouho by měl projekt běžet?
JF: Tři roky, což je průměrný cyklus podobného projektu. Potřebujeme čas na laboratorní činnost a také na přípravu dokumentace a dalších věcí, které umožní výrobu. V samém závěru bychom rádi spustili vlastní klinické hodnocení.
Administrativa asi bude asi o dost složitější než u „běžné“ experimentální léčby typu chemoterapie?
JF: Je tam hodně práce spojené s výrobou a jejím schválením v čistých prostorech. I klinické studie, které plánujeme, jsou sponzorované ÚHKT, takže je celé musíme zprocesovat, připravit a nechat schválit SÚKL, což děláme vlastními zdroji. Nicméně celý proces jsme již několikrát úspěšně dokončili.
Foto: ÚHKT
Michaela Koubová