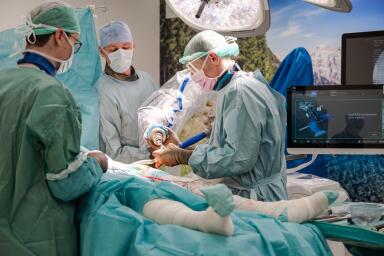
Třináct léčivých přípravků na vzácná onemocnění letos vyrazilo na doposud neprošlapanou tzv. „třetí cestu“ vedoucí ke schválení úhrady z prostředků veřejného zdravotního pojištění. Nový mechanismus pro hodnocení a posouzení úhrady orphanů (vedle standardního správního řízení a řízení pro vysoce inovativní léčivé přípravky) přinesla novela zákona o veřejném zdravotním pojištění platná od začátku tohoto roku. Na hlubší vyhodnocení jeho fungování je ale stále ještě příliš brzy, shodli se účastníci kulatého stolu Zdravotnického deníku. Zatím toho totiž víme velmi málo o rozhodování v druhé – zcela nové – fázi řízení, tedy o jednání poradního orgánu ministra zdravotnictví. Ten zatím zasedal a rozhodoval (pozitivně) pouze jednou.
Po jedenácti měsících je na větší vyhodnocení funkčnosti nového typu řízení pro vyhodnocení a stanovení úhrady pro léky na vzácná onemocnění ještě brzy, stále se učíme, shodli se včera účastníci kulatého stolu Zdravotnického deníku, který se zabýval fungováním novely zákona o veřejném zdravotním pojištění platné od letošního ledna. Větší zkušenosti chybí zejména s druhou fází této „třetí cesty“, tedy jednáním poradního orgánu ministra zdravotnictví. „Víme zatím, jak funguje SÚKL, a to dle předpokladů. Ale zatím toho víme velmi málo o činnosti poradního orgánu. Ke skutečnému vyhodnocení celého procesu potřebujeme tak deset, patnáct finálních rozhodnutí,“ je přesvědčený ředitel společnosti Value Outcomes Tomáš Doležal.

Zleva: ředitel společnosti Value Outcomes Tomáš Doležal, výkonný ředitel Asociace inovativního farmaceutického průmyslu David Kolář, místopředseda České asociace pro vzácná onemocnění René Břečťan a ředitelka Státního ústavu pro kontrolu léčiv Irena Storová.
První schválený lék je trochu atypický
Správní řízení podle §39da zákona, jak z ní oficiální název oné „třetí cesty“, zavádí několik zcela nových prvků. Předně rozděluje řízení do dvou fází – hodnocení, které probíhá na Státním ústavu pro kontrolu léčiv (SÚKL), a posuzování, jež se přesouvá na ministerstvo zdravotnictví. Dále do procesu formálně zapojuje do té doby nevídané subjekty – pacientské organizace a odborné společnosti. Ty hrají důležitou roli především v hodnocení nákladů a přínosů léku z pohledu celospolečenské perspektivy a kvality života pacienta a jeho okolí. To je je zcela nový pohled, který částečně odsouvá do pozadí do té doby klíčový parametr – nákladovou efektivitu přípravku. Konečné rozhodnutí o úhradě vychází z vyhodnocení celkem deseti kritérií vyjmenovaných zákonem.
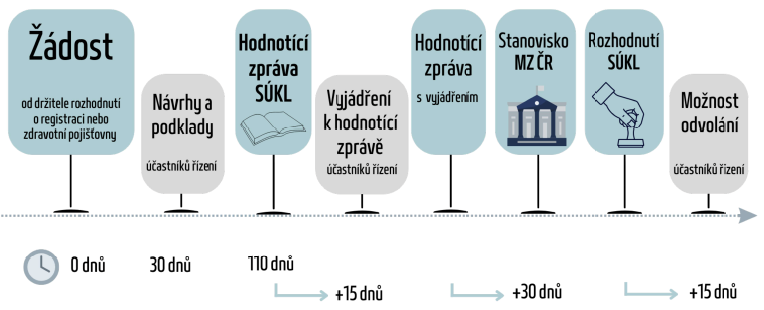
Po jedenácti měsících je zřejmé, že tento nový proces se rozbíhá spíš pomaleji. Celým řízením zatím úspěšně prošel jen jediný přípravek k léčbě spinální svalové atrofie. A ten je ještě trochu atypický, protože již v době schválení řádné úhrady byl potřebným pacientům hrazen na základě individuálních žádostí o úhradu podle paragrafu 16. „Teď začnou do řízení vstupovat léky, které nemají úhradu a často se nepovolují ani přes paragraf 16 nebo jen v minimálních případech,“ upozornila ředitelka odboru léčiv Všeobecné zdravotní pojišťovny ČR Alena Miková.

Dnes je již ve fázi hodnocení dalších jedenáct přípravků, ty však ještě nedoputovaly na stůl k projednání oním poradním orgánem ministra zdravotnictví. Podle ředitelky odboru léčiv a zdravotnických prostředků ministerstva zdravotnictví Daniely Rrahmaniové je ale již i z jeho prvního výstupu zřetelné několik skutečností. „Poradní orgán dal jednoznačně najevo, že bude požadovat větší míru detailu u komparátorů. Je zřejmé již dnes, že si vynutí kultivaci prostředí,“ uvedla. S tím souhlasí i zástupce pacientů a místopředseda České asociace pro vzácná onemocnění René Břečťan: „Již to první rozhodnutí přineslo hodně impulsů,“ konstatoval.
Podle člena předsednictva České lékařské společnosti JEP a profesora farmakologie Jana Švihovce, který se zatím jediného jednání poradního orgánu osobně zúčastnil, je zřejmé, že si jeho členové budou muset ještě nastavit vnitřní pravidla pro své rozhodování. „Očekávám diskusi jen k tomuto tématu,“ uvedl Švihovec.

Ještě bych to nechala si sednout
„Myslím, že jsme se k tomu postavili úspěšně čelem a doufám, že takto budeme pokračovat i nadále. Za nás neidentifikujeme žádné procesní problémy,“ je přesvědčená ředitelka SÚKL Irena Storová. Výkonný ředitel Asociace inovativního farmaceutického průmyslu David Kolář nicméně připouští, že se „narazilo na místa, na nichž se aplikačně neshodneme. Musíme se o tom dále bavit,“ zdůraznil.
Podle předsedkyně Lékové komise Svazu zdravotních pojišťoven ČR Kateřiny Podrazilové je ještě brzy na úvahy o případné další legislativní úpravě. „Je ale zřejmé, že některé problémy se začínají krystalizovat a o nich je třeba se bavit,“ dodala.

Daniela Rrahmaniová připouští, že ministerstvo zdravotnictví obdrželo řadu podnětů na zlepšení. „Předpokládám, že po novém roce zahájí práci nějaká pracovní skupina, která se pokusí novelu zušlechtit. Ale zatím bych se přimlouvala za to nechat si to ještě trochu sednout,“ uvedla na závěr.
Helena Sedláčková
Mohlo by vás zajímat
Foto: Radek Čepelák
Diskuzi na kulatém stole se budeme podrobněji věnovat v dalších článcích.
Kulatý stůl se konal s laskavou podporou Asociace inovativního farmaceutického průmyslu.